更新時間:2020-05-12
奶牛健康管理專家Todd Meyer(馬國達)博士在第四屆國際畜牧業創新論壇——規模化牧場奶牛營養、繁殖、健康管理峰會上,做了題爲“奶牛布氏杆菌病”的專題講座,通過布氏杆菌基本情況介紹,介紹了布病的檢測方法,爲牧場找尋出最适合的檢測方法,并介紹了目前使用的疫苗及使用方法。

長按圖片保存可分享至朋友圈
馬國達博士首先帶大家了解了布病的簡史。大約2500年前,希波克拉底時期在地中海地區的綿羊和山羊中首次被發現。英國外科醫生大衛布魯斯博士于1887年首次從馬耳他的感染者身上分離出梅利特布氏杆菌,布氏杆菌是以他的名字命名的。伯納德·邦(丹麥)博士于1897年首次從牛身上分離出流産型布氏杆菌,家畜布氏杆菌病被廣泛稱爲Bang病。約翰巴克博士(美國農業部)重新檢查了他在辦公桌上放了一年的流産型布氏杆菌培養物,看發生了什麽,他觀察到第19個培養皿中有一個突變株,其毒性較小,這成爲了S19疫苗,S19于1941年首次使用。S19布氏杆菌最初是從一頭名叫“馬蒂爾達”的娟珊牛身上分離出來的。從那以後,疫苗接種(S19和RB51主要用于牛)和檢測是全世界控制和根除布氏杆菌病程序的關鍵。很少有國家能在動物種群中徹底消滅這種疾病,每年全世界大約有50萬新感染的人類感染病例。盡管全球關注控制和預防,但該病仍在許多國家和地區流行。
爲何布氏杆菌病如此難以控制?首先,它能良好的适應宿主也就是牛。很好的隐藏在免疫系統中不受免疫系統的攻擊。對于我們的來說很難檢測和移除。大量攜帶者處于無臨床症狀狀态或潛在感染。同時,這個潛伏期不固定,有可能時間很短也有可能時間很長。複雜的免疫過程會混淆檢測結果與疫苗效果(有時候我們使用活苗會混淆檢測結果,難以治療)。同樣,布病的管控方案和根除方案難以實施。
我們能從130年的科學積累中學到什麽?50多年前的許多用于控制和管理的基本工具在現在仍被廣泛使用。比如,S19疫苗依然在全世界廣泛應用,凝集試驗(血清凝集試驗、虎紅檢測等)、補體結合檢測依然是應用最廣泛的方法。我們學習根除計劃的田間試驗中通過觀察了解了畜群天然疾病如何在牧場成長。同樣我們可以從攻毒實驗和疫苗接種效果的研究确定在遏制疫情和使用疫苗方面的預期。攻毒實驗現在全世界不太允許進行,所有我們現在看到的數據大多是50年前的數據,但依然可以學到很多東西。本報告中提到的大部分工作是在1950-1990年間完成的。
30-70年前的研究還是相關的!我們科學研究的曆史還很短,但要從過去的經驗學很多東西。了解過去有助于我們明白哪些新的信息是有用的。需要強調下攻毒實驗因爲生物安全問題,這項研究中的大部分已經不在世界任何地方進行了。
/ 布氏杆菌病的基本情況 /
布氏杆菌不會在宿主外複制,離開宿主是不會生長的。一旦進入環境,細菌就相對不穩定,生存能力有限(溫暖幹燥的環境會迅速殺死細菌)。傳播風險主要是來源牛流産或牛正常産犢釋放的大量細菌所緻。所以布病是牧場管控環境的一個重要點。我們牧場的管控主要是管控傳播途徑。隔離受感染的牛,移除、填埋胎盤和排出的液體,清潔、消毒産犢區域對于減少新感染和打破感染周期都至關重要的。
流産或正常分娩的受感染奶牛的胎盤和體液是目前主要的感染源。一克胎盤子葉含有100,000,000,000 (1千億)個生物體細菌 ,胎盤中有1,000克的子葉,一個胎盤含有大約100,000,000,000,000 (1 兆)個生物體,感染劑量被認爲是1,000,000 (1 百萬)個生物體。 一次流産/産犢可釋放100000000(1億個)劑量的布氏杆菌,一次流産/産犢可感染1億個新動物體。所以這就是爲什麽管控牛生産或流産的排放物了,這是傳播疾病的一個重要途徑。
布氏杆菌不在牛體外繁殖的,隻能存活下來。布氏杆菌喜歡在寒冷和潮濕的環境生存。布氏杆菌在草地可以存活的,在草地冬季可以存活100天,夏季30天。在幹草中不适合生存,不大可能是畜群感染的來源。作爲青貯飼料,pH值偏低,布氏杆菌在4.5或更低的pH值下不可能存活。所以飼喂飼養不太可能成爲布病轉播的途徑。在糞便存活是要長一些的,有潛在的接觸風險的,但很少有證據證明這是一種重要的感染源。
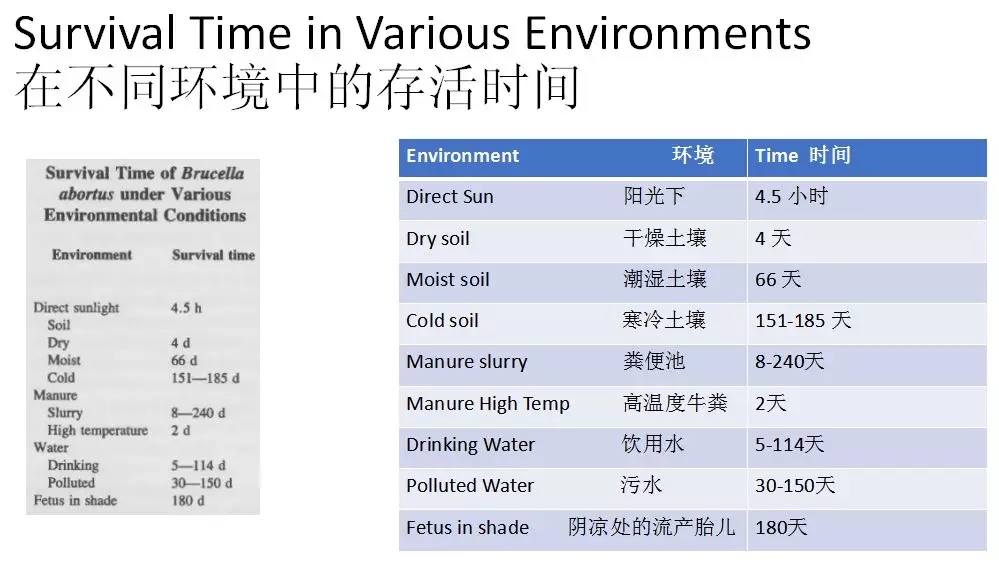
上圖的調查數據顯示,布氏杆菌在陽光下和幹燥土壤中存活時間很短,在潮濕的土地上可以存活66天,在寒冷的土壤裏可以存活2-3個月,在糞便中(受溫度的影響)可以存活8天到4個月,在水中存活時間最長,能夠存活3-4個月,在死亡的胎兒上(避免陽光直射)可以存活180天。
▨布氏杆菌病通過牛奶的傳播
大部分的人是擔心布病通過牛奶傳播,約80%的布氏杆菌感染牛發生乳腺慢性感染,乳腺感染導緻間歇性排毒布氏杆菌到牛奶中,可能持續數年,在産奶期的第一周(初期),細菌的含量可高達200000/ml,慢慢随後降至<2000/ml,這對于工人和消費者食用未經巴氏消毒的乳制品帶來了感染風險。雖然對于一個成母牛和另一個成母牛這不是一個常見的傳染來源。但我們要把感染奶牛的牛奶飼喂犢牛是可行的傳染途徑。所以在飼喂犢牛時一定要經過巴氏殺菌。
▨布氏杆菌存在潛在感染
布氏杆菌存在潛在感染,在牛首次産犢前,經常出現青年牛檢測陰性,但該青年牛可能是過去感染性接觸的無症狀攜帶者,這是檢測和屠宰計劃失敗造成的,在這些計劃中,陽性動物全部被出售,但當被感染動物的後代再次産犢時,疾病依然存在,出現這些感染的一個可能的情況是犢牛早期暴露和菌血症,随後細菌進入淋巴組織并處于休眠期,直到再次出現第二種菌血症,并有可能侵入懷孕子宮。盡管犢牛可能通過子宮内,分娩期間,初乳和牛奶暴露感染,但一般認爲犢牛對新的感染有很強的抵抗力,直到他們懷孕的最後三個月。
▨潛在感染多常見?
這個問題無法完全回答。根據文獻由陽性母牛生的犢牛有高達10%的潛在感染率(Fensterbank,1978年),另一個在英國的研究中有2.5%的潛在感染率(Wilesmith,1978年),這是基于當時可用的檢測,這兩個文獻是在7/8年以前。由陰性母牛生的犢牛也有潛在感染的風險,這表明出生後暴露風險也是一個感染因素。在受感染的牛群中,很難區分潛在感染和在妊娠晚期或産犢前形成的感染。一胎産奶牛的高比例感染可能是由于潛在感染和快速爆發感染共同造成的(未感染動物暴露于産犢或流産造成污染的高危牛群中)。
馬國達博士介紹了攻毒實驗、大型田間試驗和Nicoletti 1977在佛羅裏達田間試驗,通過實驗總結得出:大型奶牛場在管理上更難控制疫情爆發。大于500頭規模的奶牛場往往新感染率高而且淨化很慢不容易控制疾病爆發,大型牧場很難分離已知感染的奶牛,血清陰性的攜帶者可在分娩或流産時感染許多牛,對大型牧場來說,更難打破新的感染周期。當檢測無效時(缺乏先進的檢測方法),給全群成母牛免疫(犢牛期間沒有免疫過的)是很有用的。

通過對新西蘭6個牧場的試驗研究發現:慢性感染牛群的表現可能不同于典型的新爆發牛群。慢性感染牛群的臨床流産率可能不會異常高(接種疫苗,自然接觸可提高免疫力并降低嚴重程度)。産犢前的感染可以解釋爲何産犢時培養結果陽性和血清學陰性,感染潛伏期可能是産犢前血清學陰性的原因。大量受感染的動物可能出現臨床正常,血液檢測呈陰性,但是依然傳播細菌。血清學檢測并不總是一緻的,需要多次測試(由于傳統檢測的敏感性和特異性低)。
/ 布病的檢測 /
布病的檢測過程非常複雜,因爲細菌能夠隐藏在組織中。“金标準”檢測是對生物體進行細菌培養(細菌培養很緩慢,可能造成假陰性;在胎盤/子宮分泌物、牛奶、胎兒或淋巴結中可發現細菌),在現實中這不可能實現,現在牧場真正應用的現場診斷依賴于血清學,許多受感染的奶牛在流産或正常産犢前都沒有檢測出陽性,這使得它在确認感染之前可以傳播給牛群。
▨布病的基礎免疫檢測
一般使用傳統檢測虎紅檢測,還有标準試管凝集試驗、補體結合試驗。傳統的檢測使用完整的S(光滑)布氏杆菌細胞或S-脂多糖抗原(S-LPS)提取物。而現在新的檢測核心O-多糖抗原,這種檢測可以通過熒光偏振法、一些酶聯免疫吸附檢測。這種檢測更敏感、更準确可以給淘汰牛帶來更多指導意義。另外,這些抗原存在于田間菌株和S19疫苗中,都可以被檢測陽性。所以牧場進行S19疫苗免疫,傳統上的檢測将沒有意義。
▨流行病學檢測定義
靈敏度定義是檢測出陽性是牛群中真實陽性。也就是說牛群真能檢測出陽性的多少。特異性是檢測出陰性真實陰性的數,也就是說牛群中真正挑出陰性的牛。
案例:
5000頭牛的牧場,檢測疾病發生率與檢測靈敏度和特異性的關系。有效管理方案受到檢測敏感性和特異性的影響。
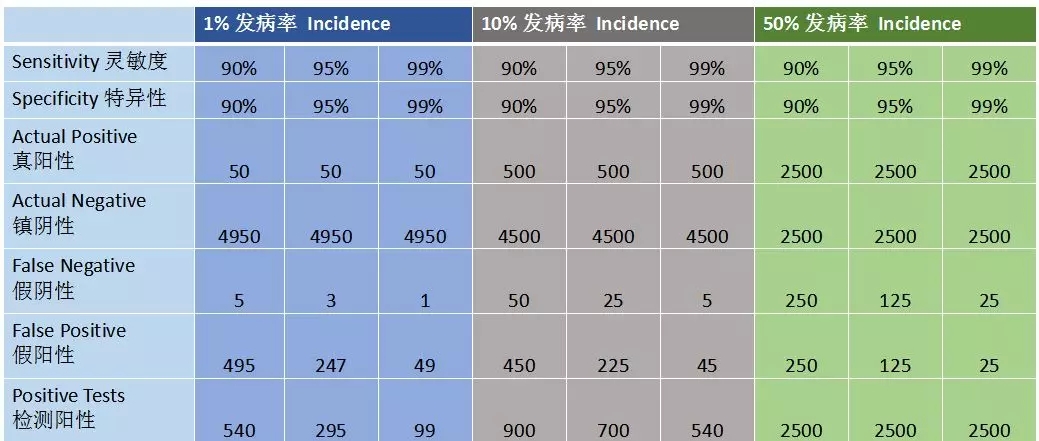
假設1%、10%、50%三種發病率情況,靈敏性、特異性都設置爲90%、95%、99%三個值,通過發病率可以算出真陽性、真陰性比例。通過靈敏性定義去算這裏面多少是假陰性、假陽性。按照5000頭牧場1%發病率情況,如果檢測的靈敏性、特異性都是90%,會檢測出4950頭陰性牛,其實隻有50頭是真陽性,會有5頭假陰性,意味着會有495假陽性出現,如果這個牧場采用檢測加淘汰清理布病的情況下,這個牧場可能就會關門了。這就意味着對于牧場實行淘汰方案檢測準确的重要性。比如檢測靈敏性、特異性提高到99%,檢測陽性隻有99頭了,你淘汰的就少了,所以理解檢測的作用是非常重要的。同時,有效管理方案受到檢測敏感性和特異性的影響。
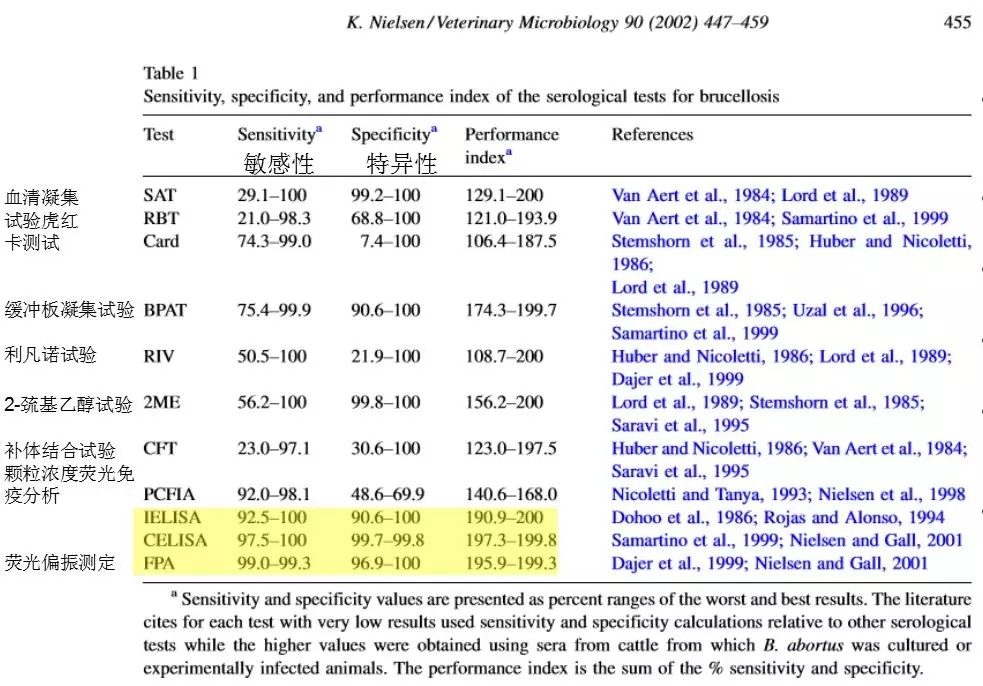
上圖是根據各種文獻進行整理後得出的敏感性和特異性。靈敏性推行的範圍是非常大的,從30%到100%,數值這麽低一定受到了其他因素的影響,但是我們經常可以發現有些檢測的靈敏性和特異性過低,所以你不能基于它進行淘汰和檢測。這也是爲什麽前面幾個用傳統方法控制布病失敗的原因。圖中用黃色加亮的這部分是熒光偏振法和Elisa,數據顯示在真實的田間或者牧場,這些檢測的靈敏性和特異性聚在一個很高的水平。試驗證明,常見檢測的敏感性和特異性,最有效的檢測方法是熒光偏振法和Elisa。
選擇檢測的标準參考以下幾點:
1.高敏感性(發現陽性奶牛)
2.高特異性(避免假陽性和不必要的淘汰)
3.便宜(更低的成本可以支持更頻繁的檢測)
4.方便(易在農場實驗室進行,可重複可定量)
我個人建議是Elisa和熒光偏振法,比較适合牧場的檢測。
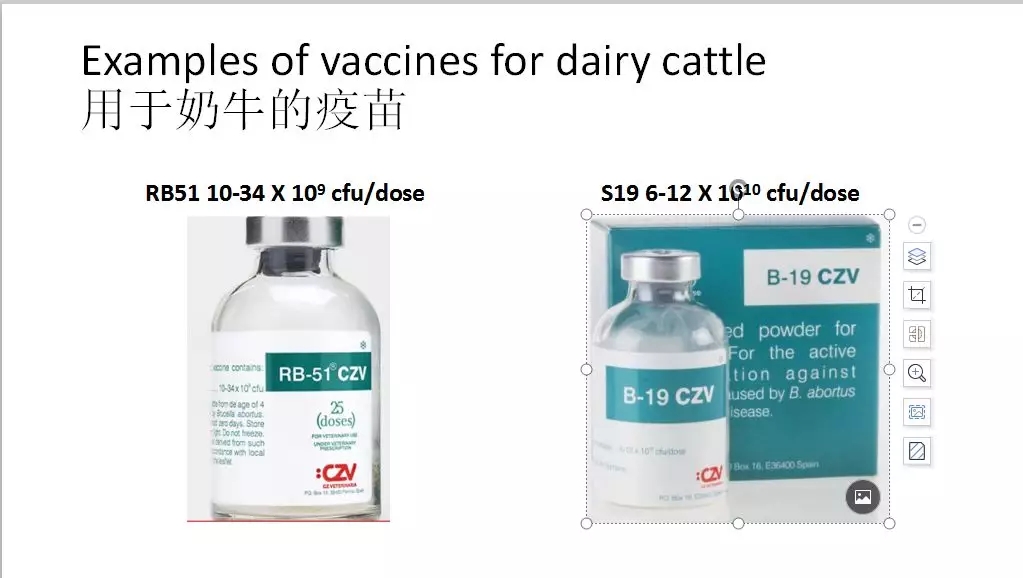
照片所顯示的是市面上常見的RB51和S19疫苗。
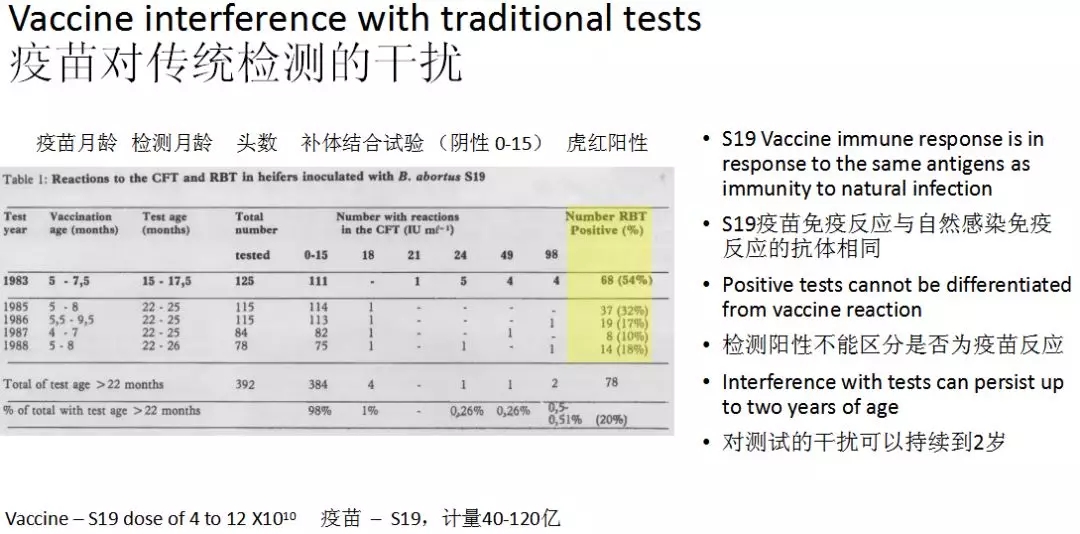
疫苗免疫會對傳統檢測有一些幹擾,注射疫苗的時間大概是4月到8月之間,檢測時間除了第一個是在15個月到17.5個月,其他都集中在22到26個月之間,應用的疫苗是S19,這裏應用的檢測是虎紅檢測,在第一個15個月到17.5個月中,50%的檢測是陽性,也就是疫苗注射後的十個月;如果把檢測推後的話,檢測陽性值要低很多,但還是在20%左右,這就是對疫苗檢測的幹擾。即使在剛産犢的時候,我們依然會檢測出很多陽性。所以你不能基于這個檢測結果就對牛進行淘汰處理,因爲有可能是疫苗反應。而熒光偏振法就可以給大家一個數量級的結果,你可以通過這個數量級分析是疫苗免疫産生的陽性還是真正被感染的結果。
RB51疫苗是由流産布氏杆菌的一種有毒形式的粗糙突變株制成,該疫苗株缺乏在田間株細胞壁中發現的脂多糖O側鏈。接種過疫苗的動物對檢測成陰性結果,這使得繼續檢測流程不受影響,常用于包括美國在内的許多國家。有報告顯示,出現過在接種布氏杆菌S19和RB51疫苗後持續感染,偶爾能從接種過疫苗的牛的牛奶、胎盤和胎兒中分離出疫苗菌株。一項研究發現,在接種S19疫苗後9-12個月内,有2.5%的牛體内有活細菌,持續性疫苗接種感染的估計值在1/100000劑量到大約0.5%之間變化很大。
在許多情況下,疫苗的持續感染僅限于淋巴結和乳腺,通常不會造成傷害。疫苗菌株是對在懷孕子宮中發現的一種糖赤藓糖醇敏感的突變品種。然而,疫苗菌株可能變回能夠定植子宮的赤藓糖醇耐受菌株,并導緻臨床流産和模拟田間菌株感染的感染。這些突變的疫苗株在S19和RB51導緻的流産中都被發現過。疫苗接種時的劑量、年齡和妊娠期可能是疫苗感染的潛在因素。

美國曾經報導了一篇人類喝未經巴氏消毒的造成的RB51布病感染,在過去的幾年中一共出現了三個案例。所以,在美國直接去喝生奶的人隻是少部分,所以這個感染大概率是由環境造成的,并不是因爲生奶。
▨管理在布病管控中的作用
牧場的管理在布病防控中非常重要,這是一個場長需要做的部分。除了疫苗接種和檢測之外,牧場還必須實施管理措施,打破新感染的周期,減少感染劑量至關重要(感染劑量幾乎完全是由于受感染奶牛流産或産犢造成的),盡快識别、隔離或淘汰陽性動物,采取隔離和檢測等所有方法減少陰性牛接觸的細菌的風險,做好高風險地區的衛生管控,防止受感染的動物再次在牧場産犢(淘汰或禁止配種)。
▨牛場的衛生管理
布魯氏杆菌病是人畜共患的疾病,工人的安全是至關重要的,當你處理陽性牛的時候要始終穿戴個人防護裝備。
密切監測懷孕晚期和産房的異常産犢情況(産房和圍産區)。産犢後期的牛以及産房需要格外的關注,隔離已知陽性牛在特定區域産犢,産房分爲多個獨立的小區遠比一個開放的區域風險小,安全的丢棄處理胎盤并用土覆蓋污染區域,在産犢後的四周是感染風險最大的,産後把陽性牛和可疑牛分離應飼養4周,一定要将犢牛盡早與母牛和其他犢牛分離開,然後單獨飼養,犢牛島是一個很好的方案。所有的初乳和常奶一定要飼喂巴殺過的牛奶。
▨疫苗保護與暴露
“如果環境中的細菌量增加10倍,疫苗的保護程度可從大約70%降低到50%,因此,很明顯,隻有正确的免疫流程配合良好的管理才能增加免疫成功的概率。最危險的時期是在流産和正常産犢時以及之後的一段時間,在隔離的區域産犢可以有效的控制疾病的傳播”。 這句話是一位醫學博士在50年前說的,我非常認同,我們不僅要有正确的疫苗,還要配合管理流程,才能達到更好的免疫效果。最危險的就是在流産和正常産犢及産犢之後的這段時間,所以這些傳染可以被很好地控制,如果你隔離出産犢區域(單獨爲陽性牛),我們要遵循良好的管理方案才能控制疾病。

長按圖片保存可分享至朋友圈
文章來源:奶牛微刊